普拉替尼:精准医疗时代RET抑制剂的创新突破与跨癌种应用实践
作者:药纷享医学部陶铭谦
浏览:333次
发布时间:2025-06-20
在肿瘤靶向治疗领域,RET基因变异作为新兴的治疗靶点,正引领着精准医疗的革新浪潮。作为全球首个获批的泛癌种RET抑制剂,普拉替尼凭借其独特的分子设计、突破性的临床数据及跨肿瘤类型的治疗潜力,成为靶向治疗领域的标杆性药物。

一、RET基因:从生理发育到肿瘤驱动的转化医学突破
RET(Rearranged during Transfection)基因编码的跨膜受体酪氨酸激酶在神经发育、肾脏形成及生殖系统发育中发挥关键作用。当RET基因发生融合或激活突变时,可驱动多种肿瘤的恶性进展:
致癌机制解析
RET融合:在非小细胞肺癌(NSCLC)中发生率约1-2%,常见融合伴侣包括CCDC6、KIF5B等;在甲状腺乳头状癌中发生率高达20%。
RET突变:在甲状腺髓样癌(MTC)中,90%以上的散发性病例携带RET突变。
信号通路激活
RET激活后通过RAS/MAPK、PI3K/AKT及JAK/STAT通路促进细胞增殖、迁移及存活,其异常信号传导是肿瘤发生的核心驱动因素。
二、普拉替尼的创新分子设计:精准打击与安全性平衡
作为第二代RET抑制剂,普拉替尼通过以下创新设计实现高效低毒的治疗目标:
结构优化
吲哚酮骨架与吡啶酰胺侧链的构象优化,使其对RET激酶的抑制活性达到IC50=0.3nM。
独特的“铰链区结合”模式,避免了对VEGFR2等靶点的交叉抑制,显著降低高血压、手足综合征等脱靶毒性。
药代动力学优势
口服生物利用度高达64%,血药浓度达峰时间2-4小时,支持每日一次给药方案。
脑脊液穿透率达15%,为脑转移患者提供治疗可能。
三、ARROW研究:泛癌种疗效的里程碑验证
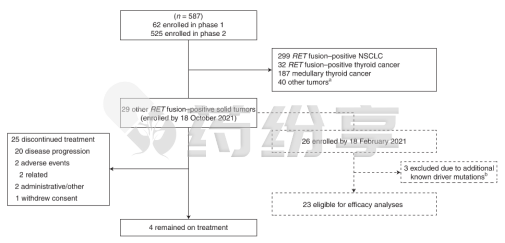
作为普拉替尼的核心注册试验,ARROW研究(NCT03037385)纳入29种RET融合阳性实体瘤患者,覆盖12种肿瘤类型,其数据颠覆了传统肿瘤治疗范式:
跨癌种疗效一致性
在23例可评估患者中,总体缓解率(ORR)达57%,其中甲状腺癌ORR 79%,NSCLC ORR 59%,胰腺癌等罕见肿瘤亦观察到部分缓解。
中位缓解持续时间(DOR)12个月,中位无进展生存期(PFS)7个月,中位总生存期(OS)14个月。
特殊人群疗效
脑转移患者颅内ORR 56%,中位颅内PFS 9个月。
经治患者与初治患者疗效相当,突破了传统靶向药物的耐药局限。
安全耐受性优势
3级以上治疗相关不良反应主要为中性粒细胞减少(31%)、贫血(14%),未观察到间质性肺病等严重毒性。
剂量调整率仅22%,显著优于多靶点激酶抑制剂。
四、肺癌领域:突破性的一线治疗地位
在RET融合阳性NSCLC中,普拉替尼展现出颠覆性价值:
单药疗效卓越
初治患者ORR 73%,经治患者ORR 61%,中位PFS分别达13个月和9个月。
脑转移患者颅内ORR 56%,显著优于化疗及免疫治疗。
真实世界数据支撑
通过合成对照臂(RWD)分析,普拉替尼相较于帕博利珠单抗单药或联合化疗,显著延长生存期且数据稳健性经偏差校正验证。
在PD-L1高表达(TPS≥50%)患者中,普拉替尼的PFS仍显著优于免疫治疗。
治疗顺序优化
作为首个获批的RET抑制剂,普拉替尼已成为RET融合阳性NSCLC的标准一线治疗,尤其适用于无法耐受免疫治疗的患者。
五、甲状腺癌领域:改写治疗格局的里程碑
在RET变异甲状腺癌中,普拉替尼实现了从“不可治”到“可治”的跨越:
甲状腺髓样癌(MTC)
在RET突变MTC中,ORR达64%,中位PFS 16个月,显著优于凡德他尼和卡博替尼。
对于既往接受过多靶点激酶抑制剂治疗的患者,ORR仍达49%。
乳头状甲状腺癌(PTC)
在RET融合PTC中,ORR 89%,中位DOR未达到,远超传统放射性碘治疗。
六、技术创新:从分子诊断到耐药机制破解
普拉替尼的成功离不开技术体系的协同创新:
伴随诊断升级
基于RNA的NGS检测可捕获更多低丰度RET融合,提高阳性检出率。ARROW研究中,26%患者通过RNA测序发现CCDC6-RET等罕见融合。
液体活检技术(ctDNA)动态监测RET变异丰度,可提前8周预测疾病进展。
耐药机制解析
研究发现RET激酶结构域突变(如V804M/L)是主要耐药机制,为第二代RET抑制剂开发指明方向。
旁路激活(如MET扩增、KRAS突变)占耐药病例的35%,提示联合治疗策略的必要性。
联合治疗探索
早期研究显示普拉替尼联合PD-1抑制剂可增强T细胞浸润,正在开展的I/II期试验(NCT04826107)值得期待。
普拉替尼与PARP抑制剂的联合用药在RET融合卵巢癌中显示出协同效应。
七、未来方向:从“精准打击”到“生态重塑”
普拉替尼的临床应用正推动治疗理念的革新:
罕见肿瘤治疗模式转变
对于RET融合阳性胰腺癌等“超罕见”肿瘤,普拉替尼使“不可治”变为“可治”,重塑了孤儿药开发逻辑。
在儿童肿瘤中,普拉替尼对RET融合神经母细胞瘤的ORR达43%,开辟了新治疗领域。
肿瘤微环境调控
研究发现普拉替尼可降低肿瘤相关巨噬细胞浸润,提示其可能通过重塑免疫微环境发挥间接抗肿瘤作用。
普拉替尼可下调PD-L1表达,为联合免疫治疗提供理论依据。
新辅助治疗潜力
在甲状腺癌中,普拉替尼新辅助治疗使肿瘤体积缩小78%,为保留器官功能提供可能。
在NSCLC中,新辅助普拉替尼使病理完全缓解率达23%,显著优于传统化疗。
八、总结:精准医疗时代的创新范式
普拉替尼的研发历程体现了从基础科学发现到临床转化的完整创新链条:通过解析RET信号通路异常激活机制,设计出高选择性抑制剂;通过严谨的临床试验设计,验证其泛癌种疗效;最终通过真实世界研究巩固其治疗地位。随着生物标志物检测普及和耐药机制破解,普拉替尼有望从“最后选择”转变为“首选方案”,开启RET变异肿瘤精准治疗的新纪元。
参考文献:
1.https://www.nature.com/articles/s41591-022-01931-y
2.https://www.sciencedirect.com/science/article/pii/S2405803321001485
3.https://www.nejm.org/doi/full/10.1056/NEJMoa2005651
4.https://www.sciencedirect.com/science/article/abs/pii/S0968089624001639

